
Individuazione di un modello collaborativo regionale per la definizione del ruolo in terapia delle innovazioni farmacologiche in oncologia utilizzando il metodo GRADE
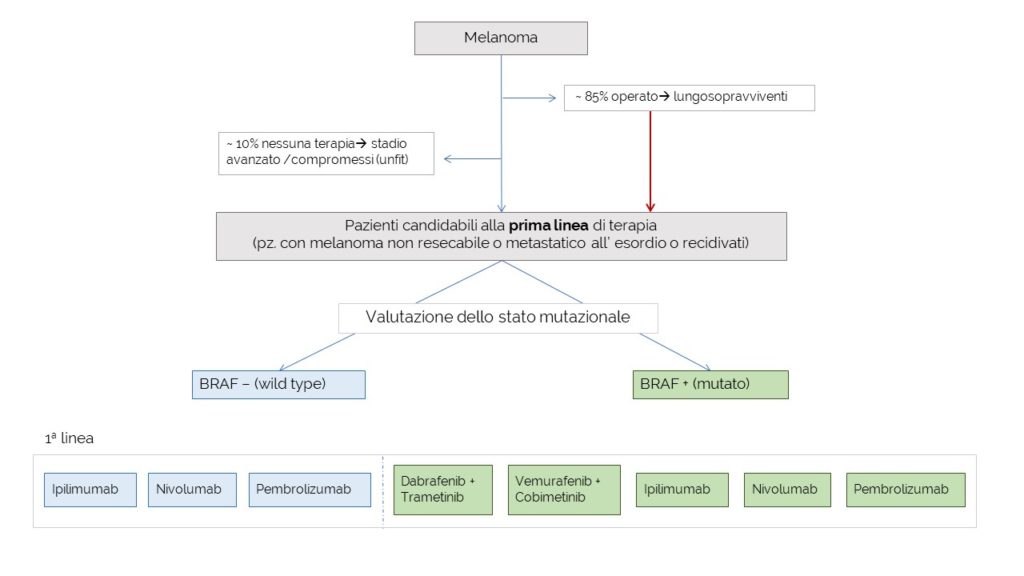
Flow chart modificato dal documento del gruppo GReFO della Regione Emilia Romagna (raccomandazione d’uso n.54 gennaio 2017 [1]).
Farmaci con indicazioni registrate e rimborsate EMA/AIFA, aggiornamento a Luglio 2017
Il melanoma è uno dei principali tumori che insorge in giovane età e in Italia è attualmente il terzo tumore più frequente in soggetti di età inferiore ai 50 anni [2]. Negli ultimi decenni l’incidenza di melanoma cutaneo è in aumento [3]: a livello mondiale si stimano 132 milioni di nuovi casi l’anno, un aumento del 15% circa rispetto al decennio precedente [4].I farmaci oncologici utilizzati per il trattamento di pazienti con melanoma avanzato, non resecabile o metastatico di recente introduzione vengono suddivisi in base allo stato mutazionale di BRAF. In particolare, per i pazienti senza mutazioni in BRAF le terapie di prima linea a disposizione sono tre:
- – Ipilimumab
- – Nivolumab
- – Pembrolizumab
Per i pazienti con mutazioni in BRAF, invece, le terapie per la prima linea sono:
- – Dabrafenib + Trametinib
- – Vemurafenib + Cobimetinib
- – Ipilimumab
- – Nivolumab
- – Pembrolizumab
Per ognuna di queste terapie sono state formulate raccomandazioni da parte di un panel multidisciplinare di specialisti con lo scopo di individuare una strategia di cura globale e formulare forza e verso delle raccomandazioni per i farmaci rimborsati dal Sistema Sanitario Nazionale e utilizzati nella singola linea di trattamento.
BIBLIOGRAFIA
- “280) Raccomandazioni evidence-based: ‘Farmaci per il melanoma avanzato, non resecabile o metastatico’ (aggiornamento gennaio 2017),” Salute. [Online]. Available: http://salute.regione.emilia-romagna.it/documentazione/ptr/elaborati/280-raccomandazioni-melanoma-avanzato-non-resecabile-o-metastatico-prima-linea-di-terapia-gennaio-2017. [Accessed: 28-Jul-2017].
- AIOM – Associazione Italiana di Oncologia Medica, “I numeri del cancro in Italia 2017,” Aiom. [Online]. Available: http://www.aiom.it/professionisti/documenti-scientifici/pubblicazioni/1,420,1,. [Accessed: 18-Sep-2017].
- F. Erdmann et al., “International trends in the incidence of malignant melanoma 1953-2008-are recentgenerationsathigher or lowerrisk?,” Int. J. Cancer, vol. 132, no. 2, pp. 385–400, Jan. 2013.
- “WHO | Skincancers,” WHO. [Online]. Available: http://www.who.int/uv/faq/skincancer/en/. [Accessed: 31-Jul-2017].
Il tumore del polmone è ancora una principale causa di mortalità legata al cancro in tutto il mondo [1]. Circa l’85% dei casi di cancro polmonare sono nello specifico casi di carcinoma polmonare non a piccole cellule (NSCLC), tumore che deriva dalle cellule epiteliali polmonari a partire dai bronchi centrali fino agli alveoli terminali e comprende diverse istologie [2]. Le tipologie più comuni di NSCLC sono il carcinoma a cellule squamose, il carcinoma a grandi cellule e l’adenocarcinoma e vengono classificate assieme in termini di approccio diagnostico, stadiazione, prognosi e per la maggior parte delle strategie terapeutiche. Oltre a queste tipologie, ce ne sono altre con una minor ricorrenza[1]. I farmaci oncologici utilizzati per il trattamento di pazienti con NSCLC in assenza di mutazione EGFR/ALK/ROS1, non resecabile o metastatico vengono suddivisi in base alla linea di terapia. I trattamenti disponibili in prima linea sono:
- – pembrolizumab per pazienti con PD-L1≥50%;
- – la combinazione pemetrexed + platino per pazienti con NSCLC ad istologia non squamosa;
- -la combinazione bevacizumab + una doppietta a base di platino per pazienti con NSCLC ad istologia non squamosa;
- -doppietta a base di platino.
In seconda linea di terapia, i trattamenti disponibili sono:
- – nivolumab
- – atezolizumab
- – pembrolizumab per pazienti con PD-L1≥1%;
- – la combinazione nintendanib + docetaxel per pazienti con NSCLC ad istologia non squamosa;
- – erlotinib;
- – docetaxel;
- – doppietta a base di platino.
Per ognuna di queste terapie sono state formulate raccomandazioni da parte di un panel multidisciplinare di specialisti con lo scopo di individuare una strategia di cura globale e formulare forza e verso delle raccomandazioni per i farmaci rimborsati dal Sistema Sanitario Nazionale e utilizzati nella singola linea di trattamento.
BIBLIOGRAFIA
- [1] Hongshu Sui, Ningxia Ma, Ying Wang, et al., “Anti-PD-1/PD-L1 Therapy for Non-Small-Cell Lung Cancer: Toward Personalized Medicine and Combination Strategies,” Journal of Immunology Research, vol. 2018, Article ID 6984948, 17 pages, 2018. https://doi.org/10.1155/2018/6984948.
- [2] R. L. Siegel, K. D. Miller, and A. Jemal, “Cancer statistics, 2017,” CA: A Cancer Journal for Clinicians, vol. 67, no. 1, pp. 7–30, 2017.
Il tumore del polmone è ancora una principale causa di mortalità legata al cancro in tutto il mondo [1]. Circa l’85% dei casi di cancro polmonare sono nello specifico casi di carcinoma polmonare non a piccole cellule (NSCLC), tumore che deriva dalle cellule epiteliali polmonari a partire dai bronchi centrali fino agli alveoli terminali e comprende diverse istologie [2]. Le tipologie più comuni di NSCLC sono il carcinoma a cellule squamose, il carcinoma a grandi cellule e l’adenocarcinoma e vengono classificate assieme in termini di approccio diagnostico, stadiazione, prognosi e per la maggior parte delle strategie terapeutiche. Oltre a queste tipologie, ce ne sono altre con una minor ricorrenza[1].
I farmaci oncologici utilizzati per il trattamento di pazienti con NSCLC in presenza di mutazione dei geni EGFR/ALK/ROS1, non resecabile o metastatico vengono suddivisi in base allo stato mutazionale. In particolare, per i pazienti EGFR mutati le terapie di prima linea a disposizione sono osimertinib, gefitinib, afatinib ed erlotinib. Per i pazienti ALK mutati le terapie di prima linea a disposizione sono crizotinib, alectinib e ceritinib. Crizotinib è disponibile anche per i pazienti ROS1 mutati. Le chemioterapie come la doppietta a base di platino (platino + gemcitabina/docetaxel), le combinazioni pemetrexed + platino e bevacizumab + doppietta a base di platino sono trattamenti di prima linea utilizzabili indifferentemente dal tipo di mutazione.
In seconda linea di terapia lo schema rimane invariato per i pazienti con NSCLC ALK e ROS1 mutati. Per i pazienti con mutazioni del gene EGFR si introduce una suddivisione delle terapie disponibili sulla base della mutazione T790M: solo per i pazienti che presentano questa mutazione è disponibile il trattamento con osimertinib, in seconda linea. Le chemioterapie come la doppietta a base di platino (platino + gemcitabina/docetaxel), docetaxel e pemetrexed sono trattamenti di seconda linea utilizzabili indifferentemente dal tipo di mutazione.
Per ognuna di queste terapie sono state formulate raccomandazioni da parte di un panel multidisciplinare di specialisti con lo scopo di individuare una strategia di cura globale e formulare forza e verso delle raccomandazioni per i farmaci rimborsati dal Sistema Sanitario Nazionale e utilizzati nella singola linea di trattamento.
BIBLIOGRAFIA
- [1] Hongshu Sui, Ningxia Ma, Ying Wang, et al., “Anti-PD-1/PD-L1 Therapy for Non-Small-Cell Lung Cancer: Toward Personalized Medicine and Combination Strategies,” Journal of Immunology Research, vol. 2018, Article ID 6984948, 17 pages, 2018. https://doi.org/10.1155/2018/6984948.
- [2] R. L. Siegel, K. D. Miller, and A. Jemal, “Cancer statistics, 2017,” CA: A Cancer Journal for Clinicians, vol. 67, no. 1, pp. 7–30, 2017.

Flow chart con la definizione del posto in terapia dei farmaci disponibili in prima linea per la leucemia linfatica cronica.
La leucemia linfatica cronica (LLC) è una neoplasia ematologica a cellule B mature caratterizzata dalla proliferazione ed accumulo di linfociti B monoclonali nel sangue, midollo, linfonodi, fegato e milza. La sopravvivenza a 5 anni pari al 85%, [1]e la sopravvivenza mediana nelle classi di età inferiori a 80 anni è più di 10 anni [2]. In alcuni soggetti la malattia è indolente, con molti anni senza necessità di terapia e speranza di vita vicina a quella della popolazione generale di pari età; in altri è aggressiva per precoce evoluzione, inadeguata risposta alla chemioterapia, ricadute in tempi brevi, sviluppo di chemiorefrattarietà o trasformazione a linfoma aggressivo. La mortalità dipende non solo dall’evoluzione della leucemia ma anche dallo sviluppo di infezioni gravi e/o opportunistiche ed alla più elevata incidenza di secondi tumori.
Per stratificare i pazienti ai fini della scelta del trattamento è necessario valutare prima di ogni terapia (di prima linea o successive) una serie di caratteristiche biologiche e cliniche, in aggiunta agli esami di routine.
Sulla base di queste caratteristiche, i pazienti verranno raggruppati nelle seguenti categorie:
- – i pazienti “fragili”
- – pazienti con citopenia autoimmune attiva.
- – pazienti con TP53 mutato/deleto.
- – pazienti “unfit” ovvero non candidabili a ricevere fludarabina, con eGFR compreso tra 40 e 70 e con CIRS>6.
- – pazienti con LLC recidivata in breve tempo (<36 mesi)
- – pazienti con fattori di rischio biologico (IGHV non mutato, del11q)
- – pazienti idonei a ricevere inibitori di BTK
BIBLIOGRAFIA
- [1] “Chronic Lymphocytic Leukemia – Cancer Stat Facts.” [Online]. Available: https://seer.cancer.gov/statfacts/html/clyl.html. [Accessed: 03-Oct-2019].
- [2] H. Brenner, A. Gondos, and D. Pulte, “Trends in long-term survival of patients with chronic lymphocytic leukemia from the 1980s to the early 21st century,” Blood, vol. 111, no. 10, pp. 4916–4921, 2008.

Flow chart con la definizione del posto in terapia dei farmaci disponibili in seconda linea per la leucemia linfatica cronica.
La leucemia linfatica cronica (LLC) è una neoplasia ematologica a cellule B mature caratterizzata dalla proliferazione ed accumulo di linfociti B monoclonali nel sangue, midollo, linfonodi, fegato e milza. La sopravvivenza a 5 anni pari al 85%, [1]e la sopravvivenza mediana nelle classi di età inferiori a 80 anni è più di 10 anni [2]. In alcuni soggetti la malattia è indolente, con molti anni senza necessità di terapia e speranza di vita vicina a quella della popolazione generale di pari età; in altri è aggressiva per precoce evoluzione, inadeguata risposta alla chemioterapia, ricadute in tempi brevi, sviluppo di chemiorefrattarietà o trasformazione a linfoma aggressivo. La mortalità dipende non solo dall’evoluzione della leucemia ma anche dallo sviluppo di infezioni gravi e/o opportunistiche ed alla più elevata incidenza di secondi tumori.
Per stratificare i pazienti ai fini della scelta del trattamento è necessario valutare prima di ogni terapia (di prima linea o successive) una serie di caratteristiche biologiche e cliniche, in aggiunta agli esami di routine.
Sulla base di queste caratteristiche, i pazienti verranno raggruppati nelle seguenti categorie:
- – i pazienti “fragili”
- – pazienti con citopenia autoimmune attiva.
- – pazienti con TP53 mutato/deleto.
- – pazienti “unfit” ovvero non candidabili a ricevere fludarabina, con eGFR compreso tra 40 e 70 e con CIRS>6.
- – pazienti con LLC recidivata in breve tempo (<36 mesi)
- – pazienti con fattori di rischio biologico (IGHV non mutato, del11q)
- – pazienti idonei a ricevere inibitori di BTK
BIBLIOGRAFIA
- [1] “Chronic Lymphocytic Leukemia – Cancer Stat Facts.” [Online]. Available: https://seer.cancer.gov/statfacts/html/clyl.html. [Accessed: 03-Oct-2019].
- [2] H. Brenner, A. Gondos, and D. Pulte, “Trends in long-term survival of patients with chronic lymphocytic leukemia from the 1980s to the early 21st century,” Blood, vol. 111, no. 10, pp. 4916–4921, 2008.
